
Extras aus dem Labor
Es gibt noch viele kleine „Stellschrauben“, an denen wir im Labor im Rahmen einer Kinderwunschbehandlung drehen können. Unserer Meinung nach gilt hier nicht „Viel hilft viel“, sondern die gezielte Optimierung Ihrer Behandlung kann Ihre Chancen auf eine Schwangerschaft zusätzlich verbessern.
Welches Verfahren für Sie das passende ist, entscheiden wir individuell mit Ihnen gemeinsam. Im Folgenden wollen wir Ihnen diese Laborverfahren vorstellen.
Laborverfahren im Überblick
Blastozystenkultur
Nach der Befruchtung der Eizelle durch ein Spermium fängt die Eizelle an sich zu teilen. Ab diesem Zeitpunkt sprechen wir von einem Embryo. In der Natur passieren diese Teilungsschritte im Eileiter auf dem Weg zur Gebärmutterhöhle. Optimaler Weise befindet der Embryo sich nach 48h im 4-Zell-, nach 72h im 8-Zell-Stadium, usw. Nach 5-6 Tagen ist der Embryo in der Gebärmutter angekommen. Nun hat er das Blastozysten-Stadium erreicht und ist bereit zu schlüpfen und sich einzunisten. Leider entwickeln sich nur etwa ein Drittel der befruchteten Eizellen überhaupt zur Blastozyste, da nicht jeder Embryo die Fähigkeit zur Einnistung und Weiterentwicklung besitzt.
Bei der Blastozystenkultur findet diese Entwicklung im Brutschrank statt. Der Embryo befindet sich bei optimalen Temperaturen in einem auf seinen besonderen Nährstoffbedarf abgestimmten Kulturmedium. Er kann dann am fünften Tag zurücktransferiert werden.
Kryokonservierung
Im Rahmen einer Stimulationsbehandlung kann es zur Gewinnung von mehreren Eizellen kommen. Die Kryokonservierung bietet Ihnen die Möglichkeit, diese Eizellen zu sichern und für einen weiteren Versuch ohne erneute Stimulationsbehandlung zu verwenden.
Auch Spermien, Hoden-oder Eierstockgewebe können zur Sicherung der Zeugungsfähigkeit über Jahre bei minus 196 Grad Celsius gelagert werden.
Wenn im Rahmen einer IVF/ICSI-Behandlung überzählige befruchtete Eizellen entstehen, können wir diese einfrieren (kryokonservieren). Mit diesen können Sie dann zu einem späteren Zeitpunkt einen erneuten Transfer planen. Das funktioniert auch noch nach Jahren, wenn Sie beim frischen Transfer direkt nach einer IVF/ICSI-Behandlung schwanger wurden.
Die Kryokonservierung erfolgt in unserem Labor über ein ultraschnelles Einfrierverfahren, der Vitrifikation. Hierbei bilden sich keine Eiskristalle, welche die Zellen möglicherweise schädigen könnten. Dasselbe Verfahren benutzen wir auch für die unbefruchteten Eizellen beim Medical oder Social Freezing.
Der Vorteil der Kryokonservierung besteht darin, dass Sie nicht erneut stimulieren müssen, weniger Belastung für Sie und Ihren Körper. Falls Sie in einem sogenannten frischen Zyklus direkt nach einer IVF/ICSI-Behandlung schwanger werden, bleiben Ihre eingefrorenen Zellen so „jung“ wie bei der Entnahme. Daraus ergibt sich für Sie eine höhere Schwangerschaftschance und eine niedrigere Fehlgeburtsrate bei einem erneuten Kinderwunsch zu einem späteren Zeitpunkt.
Kryotransferzyklen
Ein Transfer ist im Rahmen eines natürlichen Zyklus möglich
Kryotransferzyklen nennt man die Zyklen mit einem Embryotransfer aus vorher eingefrorenen Zellen. Wir begleiten Sie dabei mit einem Zyklusmonitoring in Ihrem natürlichen Zyklus. Das bedeutet für Sie, dass Sie keine Medikamente für eine Stimulation einzunehmen brauchen. Ihr Körper gibt individuell den optimalen Zeitpunkt für den Kryotransfer vor.
Bei wenigen Frauen ist die leichte Unterstützung durch Östrogene notwendig, um die Gebärmutterschleimhaut in ihrem Wachstum zu unterstützen.
Wenn Sie aus beruflichen oder privaten Gründen nur ein kleines Zeitfenster für den Kryotrasnfer zur Verfügung haben, können wir mittels der Einnahme von Östrogenen den Zeitpunkt für die optimale Schleimhautempfänglichkeit individuell mit Ihnen planen.
Der Zeitaufwand sowie die körperliche Belastung sind im Rahmen eines Kryotransferzyklus gering. Sie benötigen meist nur einen Ultraschalltermin bei uns, um den Transfertermin zu planen.
Assisted Hatching – AH
Normalerweise ist während der frühen Teilungsphase der Embryo von der Zona pellucida umgeben. Diese Hülle schützt den Embryo bei der Passage durch den Eileiter. Bevor der Embryo sich in der Gebärmutterschleimhaut einnisten kann, muss er aus dieser Hülle schlüpfen (engl. hatching). Unter „Assisted Hatching“ versteht man die künstliche Eröffnung der Schutzhülle, so dass der Embryo leichter schlüpfen kann.
Nicht für jeden Patienten*in ist ein „Assisted Hatching“ empfehlenswert. Denn der Embryo benötigt den Widerstand, der durch die Begrenzung der Hülle besteht, als Reiz für seine Zellteilung.
Bei einem kleinen Prozentsatz der Blastozysten kann die Hülle zu dick sein. Ursächlich dafür kann das Alter der Eizelle oder eine Kryokonservierung sein. In diesen Fällen profitieren die Blastozysten von einer kleinen Öffnung, die per Hightech-Laser kurz vor dem Transfer herbeigeführt wird. Die Eröffnung der Zona erfolgt in Millisekunden und ist exakt steuerbar, so dass der Embryo nicht geschädigt wird.
Calcium-Ionophor-Behandlung
In wenigen ausgewählten Fällen (z.B. einem totales Befruchtungsversagen) kann erwogen werden, den Befruchtungsvorgang während einer ICSI-Behandlung zu unterstützen. Die Eizelle wird dann unmittelbar nach der Injektion mit der Samenzelle in ein Kulturmedium mit Calcium-Ionophor eingesetzt.
Polkörperdiagnostik – PKD
Unmittelbar nach der Befruchtung gibt die Eizelle zwei Polkörper nach außen ab, die entnommen und untersucht werden können. Sie enthalten das mütterliche Erbgut, so dass die Untersuchung Rückschlüsse auf den mütterlichen Anteil des Erbgut im späteren Embryo zuläßt. Somit stellt die PKD die frühste Form der genetischen Untersuchung dar und kann möglicherweise die Fehlgeburtsrate senken.
Die PKD ist eine genetische Untersuchung, die zur Präimplantationsdiagnostik gehört, was bedeutet, dass Zellen vor der Einnistung (Implantation) des Embryos untersucht werden.
Bei der Polkörperdiagnostik (PKD) wird die Schutzhülle des Embryos (Zona pellucida) gezielt im Bereich der Polkörper eröffnet. Dies ermöglicht die schonende Entnahme dieser für die genetische Untersuchung. Die Polkörper enthalten die überzähligen ausgestoßenen mütterlichen Chromosomensätze, die nach der Befruchtung nach außen abgegeben werden. Es sind also keine Aussagen zum väterlichen Einfluß möglich.
ZyMot®
Für die Insemination oder künstliche Befruchtung ist es entscheidend, dass bei der Aufbereitung des Ejakulats nur die „besten“ Spermien isoliert werden. Mit dem ZyMot® Chip gelingt dies auf besonders schonende Weise.
Der Chip verfügt über mirkofluidische Kanäle oder Poren, welche nur von Spermien mit sehr guter Beweglichkeit passiert werden können. Diese werden so angereichert, ohne sie wie bei herkömmlichen Aufbereitungsmethoden durch die Zentrifugation zusätzlicher Belastung auszusetzen. Diese Art der Spermienselektion kommt den natürlichen Umständen bei der Befruchtung sehr nahe.
Der Begriff DNA-Fragmentierung beschreibt Brüche in der DNA der Spermien, die als mögliche Ursache für männliche Unfruchtbarkeit gelten.
Ein hoher DNA-Fragmentierungsgrad kann die Erfolgsrate bei einer künstlichen Befruchtung negativ beeinflussen, die bei der Auswahl von Spermien für die Behandlung jedoch unter dem Mikroskop nicht erkannt werden. Durch die Aufbereitung von Spermien mit dem ZyMot® Chip steigt die Wahrscheinlichkeit, dass nicht nur mikroskopisch intakte Spermien, sondern auch solche mit geringer DNA-Fragmentierung für die Befruchtung zum Einsatz kommen.
CatSper-Test
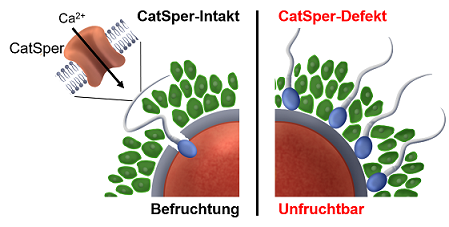
Für die Befruchtung müssen Spermien die schützende Hülle der Eizelle überwinden. Dazu schlagen sie kraftvoll mit ihrem Schwanz. Dieses Schwimmverhalten wird vom Spermien-Protein „CatSper“ gesteuert. Das Hormon Progesteron aktiviert dieses Protein. Ist CatSper defekt, bleiben Spermien in der Eihülle stecken.
EmbryoGlue
EmbryoGlue ist ein Hyaluronsäure-haltiges Embryotransfer-Medium. Vor dem Embryotransfer befindet sich der zu transferierende Embryo zunächst in einer Schale mit Kulturmedium, und wird von dort aus zusammen mit etwas Medium in den Transferkatheter aufgezogen. Der Transferkatheter wird wiederum in die Gebärmutter eingeführt, und der Embryo dort zusammen mit dem Medium aus dem Katheter herausgelassen. Ziel ist es, dass sich der Embryo in die Gebärmutterschleimhaut einnistet. Dafür ist eine Kontaktaufnahme und ein Signalaustausch zwischen Embryo und Gebärmutterschleimhaut notwendig.
EmbryoGlue kann als alternatives Embryotransfermedium verwendet werden. Das herkömmliche Medium wird dann einfach durch EmbryoGlue ersetzt. Die darin enthaltene Hyaluronsäure ist eine natürlich u.A. in der Gebärmutter vorkommende Verbindung, die bekanntermaßen eine Rolle bei der Bindung von Zellen und Geweben aneinander spielt. In unserem Kontext soll EmbryoGlue als „Kleber“ die Bindung des Embryos an die Gebärmutterschleimhaut fördern, wodurch die Einnistung erleichtert wird.
Nach aktueller Einschätzung der europäischen Gesellschaft für Reproduktion und Embryologie des Menschen (ESHRE) wird davon ausgegangen, dass die Verwendung von EmbryoGlue sicher ist. Die Erhöhung der Implantationswahrscheinlichkeit kann zwar zu einer gesteigerten Mehrlingsrate beitragen — dieses Risiko lässt sich durch die konsequente Übertragung von nur einem Embryo (SET von engl. ‚single embryo transfer‘) allerdings wirkungsvoll verhindern.
Typische Indikationen für die Nutzung von EmbryoGlue sind: Wiederholtes Implantationsversagen (RIF von engl. ‚repeated implantation failure‘), ein erhöhtes Alter der Patientin oder eine suboptimale Embryonalentwicklung.
Jetzt Termin vereinbaren
Zur Terminbuchung bei DoctolibWunschtermin nicht verfügbar?
Rufen Sie uns gerne an.
+49 211 - 950 758 0
